Endocarditis infecciosa: Etiología, patogenia, clasificación, diagnóstico y métodos de tratamiento
Índice
La endocarditis infecciosa es una enfermedad potencialmente mortal asociada a la inflamación del endocardio, predominantemente el aparato valvular del corazón, causada por la invasión microbiana. A pesar del desarrollo de la terapia antibiótica y de las modernas técnicas de imagen, la tasa de mortalidad del total de pacientes sigue siendo elevada.
Epidemiología
La incidencia de la endocarditis infecciosa oscila entre 3 y 15 casos por 100.000 habitantes y año. La incidencia aumenta con la edad, alcanzando un máximo en los mayores de 60 años debido a la acumulación de factores de riesgo como prótesis valvulares, implantes cardíacos, enfermedades crónicas e intervenciones médicas frecuentes. Los hombres tienen aproximadamente el doble de probabilidades de padecer la enfermedad que las mujeres.
En las últimas décadas, se ha producido un cambio en el perfil epidemiológico: en lugar de cardiopatías reumáticas y consumidores de drogas intravenosas, ahora predominan los pacientes ancianos, a menudo con válvulas, prótesis y marcapasos implantados.
Etiología
La causa de la EI puede estar provocada por diversos microorganismos, entre ellos:
- Staphylococcus aureus es el líder en frecuencia, sobre todo en EI hospitalaria y en drogadictos.
- Los estreptococos viridans son agentes causales clásicos en las lesiones valvulares nativas en pacientes sin factores de riesgo evidentes.
- Enterococcus spp. – significativo en pacientes ancianos, a menudo asociado a intervenciones urogenitales.
- Los estafilococos coagulasa negativos son agentes causales frecuentes en las infecciones de válvulas protésicas.
- Con menos frecuencia: grupo HACEK, hongos, bacilos gramnegativos, etc.
Los factores de riesgo incluyen la presencia de válvulas artificiales, marcapasos, EI previa, defectos cardíacos, consumo de drogas intravenosas y hemodiálisis crónica.
Patogénesis
La patogénesis de la endocarditis infecciosa implica varios eslabones consecutivos:
- Daño del endotelio valvular (por ejemplo, por flujo sanguíneo turbulento) → exposición de la matriz extracelular.
- Adhesión de plaquetas y fibrina → formación de trombo estéril (endocarditis trombótica no bacteriana).
- Invasión microbiana: en la bacteriemia transitoria, los microorganismos colonizan el coágulo.
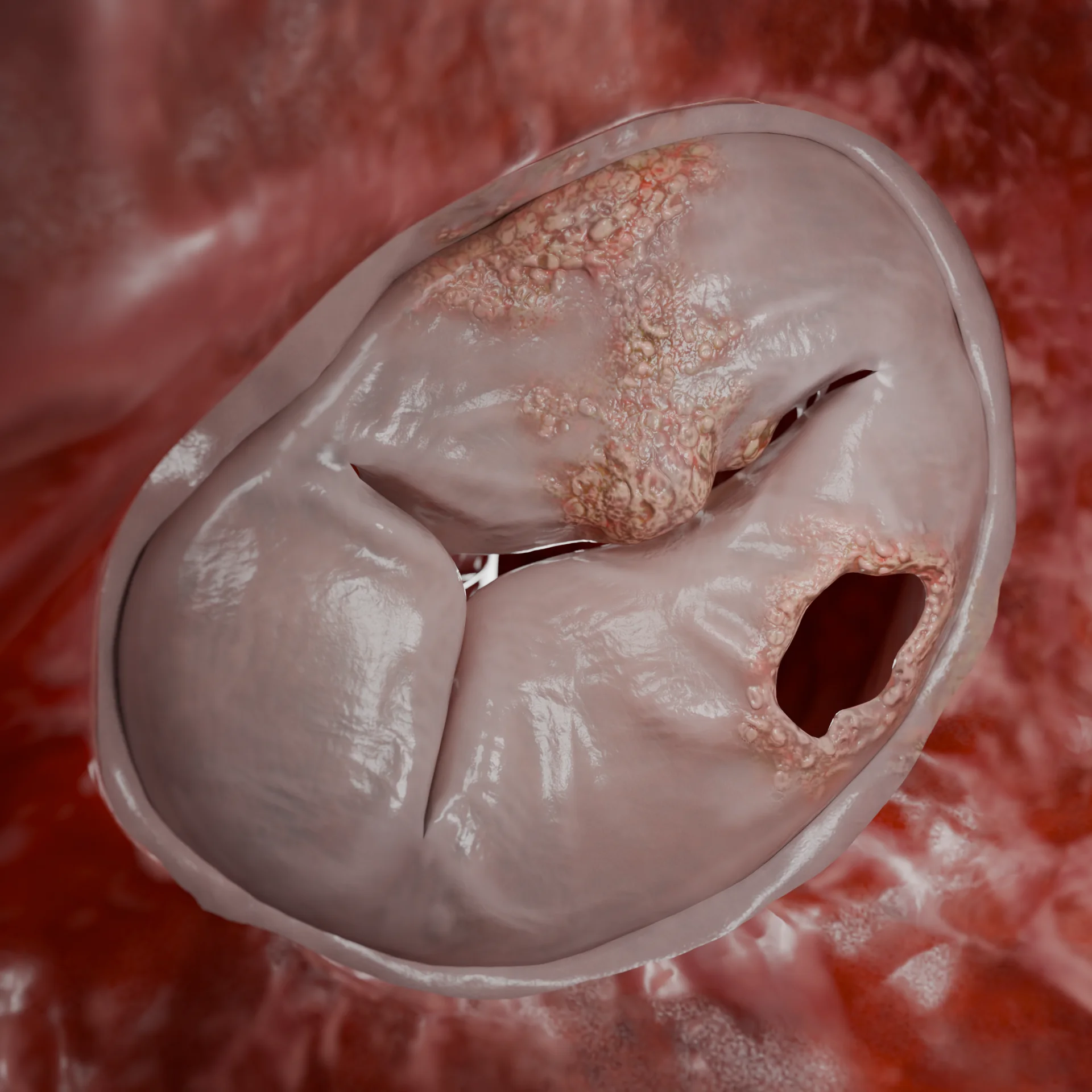
- Formación de vegetación: grupos densos de fibrina, células inflamatorias y bacterias protegidas de la respuesta inmunitaria y de los antibióticos.
- Destrucción de las estructuras valvulares y posible embolización → complicaciones sistémicas, sepsis, insuficiencia cardiaca aguda. Los mecanismos inmunitarios también contribuyen al desarrollo de complicaciones como la vasculitis y la glomerulonefritis.
El paso clave es la formación de vegetaciones que favorecen la persistencia de la infección y el desarrollo de complicaciones embólicas.
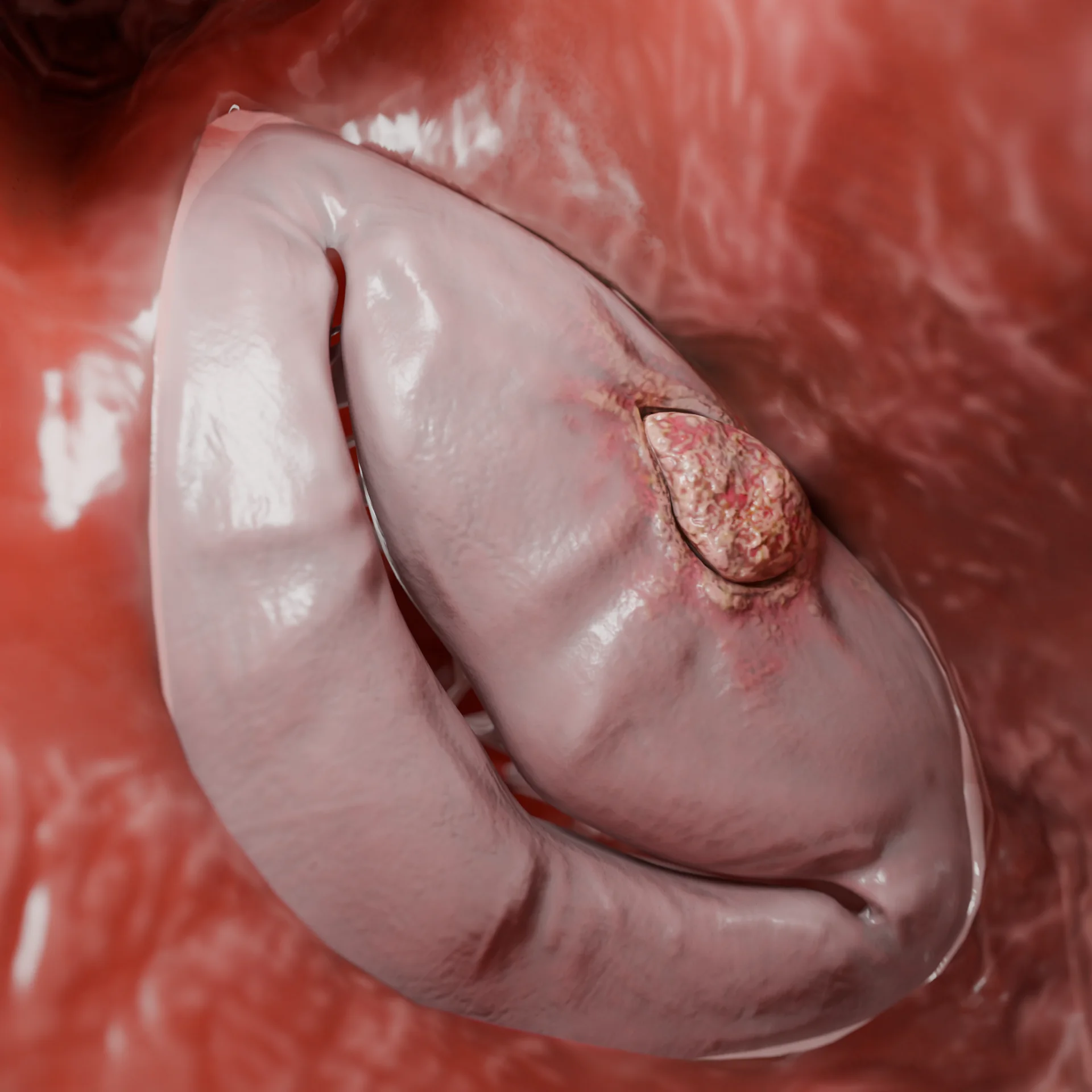
Clasificación de la endocarditis infecciosa
| Por localización del proceso: Endocarditis del lado izquierdo | Daño de la válvula mitral y/o aórtica (lo más frecuente) |
| Endocarditis derecha | Lesión de la válvula tricúspide y/o pulmonar (menos frecuente) (más común en consumidores de drogas inyectables, pacientes con CVC) |
| Combinado | Lesiones simultáneas de las divisiones derecha e izquierda |
| Endocarditis protésica | Inflamación en una prótesis valvular mecánica o biológica |
| Endocarditis por dispositivos | Infección asociada a electrodos de marcapasos, DAI, etc. |
| Por etiología (agente causal): Cocos grampositivos | Staphylococcus aureus, estafilococos coagulasa-negativos, Streptococcus viridans, Enterococcus spp. |
| Bacterias Gram negativas | Grupo HACEK, otras Enterobacteriaceae |
| Atípica/obligatoriamente intracelular | Coxiella burnetii, Bartonella spp., Tropheryma whipplei |
| Setas | Candida spp., Aspergillus spp. (poco frecuentes, más comunes en personas inmunodeprimidas) |
| Por curso clínico: Agudo | Inicio: súbito Evolución: rápida, agresiva Patógenos más frecuentes: Staphylococcus aureus, estreptococos β-hemolíticos Características: destrucción rápida de la válvula, sepsis, alta tasa de mortalidad |
| Subagudo | Inicio: gradual (semanas) Curso: lento, con sintomatología poco clara Patógenos más frecuentes: Streptococcus viridans, Enterococcus spp. Características: anemia, subfebril, manifestaciones inmunitarias. |
| Crónica | Inicio: prolongado (meses) Curso: latente o recurrente Patógenos más comunes: bacterias de baja virulencia, formas negativas al cultivo Características: inflamación prolongada, cambios valvulares persistentes, posible recaída tras la terapia |
.webp)
.webp)
Manifestaciones clínicas
La sintomatología de la EI es variable, desde inespecífica hasta potencialmente mortal:
- Los síntomas comunes de la endocarditis infecciosa incluyen fiebre, sudoración, fatiga y pérdida de peso.
- Signos cardíacos: soplo nuevo o alterado, signos de insuficiencia cardíaca.
- Complicaciones embólicas: ictus, isquemia de extremidades, infartos de órganos internos.
- Manifestaciones inmunitarias: púrpura, nódulos de Osler, manchas de Janway, glomerulonefritis.
- Lesión del sistema conductivo: bloqueos, arritmias.
- En curso grave de EI puede desarrollarse: shock séptico, fallo multiorgánico.
- En la endocarditis protésica, los soplos auscultatorios pueden ser menos pronunciados, es más probable que se desarrolle una infección perianular: abscesos, pseudoaneurismas, fístulas.
Diagnóstico de la endocarditis infecciosa
Métodos de laboratorio:
- Analítica general: anemia normocítica, leucocitosis, trombocitopenia.
- COE, PCR: Significativamente elevados.
- Procalcitonina: puede estar moderadamente elevada.
- Hallazgos renales: elevación de la creatinina (glomerulonefritis, embolia).
- Hemocultivos: ≥3 muestras separadas ≥30 min antes de los antibióticos (hasta un 95% de sensibilidad).
- Serología/PCR: para EI con cultivo negativo(Bartonella, Coxiella, Brucella, etc.).
Métodos instrumentales:
- Ecocardiografía (preferible la ecocardiografía de DP a la de TT): Vegetaciones, abscesos, pseudoaneurismas, perforaciones, disfunción protésica. Sensibilidad de la ecocardiografía de EP > 90%.
- TC: Permite detectar abscesos, pseudoaneurismas, émbolos y complicaciones de la endocarditis infecciosa.
- PET-TC: Detecta zonas de inflamación activa e infección; especialmente valioso en endocarditis protésica y presencia de dispositivos.
- Resonancia magnética cerebral: A menudo revela múltiples émbolos, incluso en ausencia de síntomas neurológicos
Criterios Duke
Un esquema diagnóstico internacionalmente reconocido para la endocarditis infecciosa (EI) que integra los hallazgos clínicos, microbiológicos y de imagen.
La probabilidad de tener EI:
- Fiable: 2 criterios principales O 1 principal + 3 criterios secundarios O 5 criterios secundarios;
- Posible: 1 mayor + 1-2 menores O 3 menores;
- Excluidos: diagnóstico alternativo, falta de confirmación en la autopsia o resolución completa de los síntomas sin tratamiento.
Criterios principales ( Criterios principales )
- Hemocultivo positivo (uno de los siguientes):
- ≥2 hemocultivos positivos de microorganismos típicos (por ejemplo, S. aureus, Streptococcus viridans, Enterococcus spp.) de diferentes muestras;
- Hemocultivo persistentemente positivo: ≥2 muestras positivas con un intervalo de ≥12 horas;
- ≥3 de 4 hemocultivos positivos tomados en 1 hora.
- Evidencia de una lesión endocárdica:
- EcoCG positivo (ECO PE o ECO TT): vegetación, absceso, pseudoaneurisma, perforación;
- Un nuevo caso de fallo valvular (insuficiencia).
- Alternativamente (ESC 2023):
- PET-TAC o SPECT positivos por sospecha de EI protésica;
- Cultivo positivo de material valvular intraoperatorio.
Criterios menores ( Criterios menores )
- Cardiopatía predisponente o administración de fármacos por vía intravenosa.
- Fiebre ≥38 °C.
- Fenómenos vasculares: émbolos, infartos, hemorragias, manchas de Janway.
- Fenómenos inmunológicos: Nódulos de Osler, manchas de Roth, glomerulonefritis, factor reumatoide.
- Hallazgos microbiológicos que no cumplen los criterios básicos: un único hemocultivo positivo o confirmación serológica de infección típica de EI.
Tratamiento de la endocarditis infecciosa
Modificación de los factores de riesgo
- Retirada/sustitución de dispositivos y catéteres infectados.
- Saneamiento de los focos de infección (dientes, piel).
- Limitar los procedimientos invasivos innecesarios.
Tratamiento farmacológico
Principios:
- Altas dosis de antibióticos bactericidas;
- Terapia prolongada (normalmente de 4 a 6 semanas);
- Ten en cuenta la CMI (concentración inhibitoria mínima);
- Enfoque individualizado en prótesis, abscesos y cepas resistentes.
Ejemplos de esquemas (según ESC 2023):
- Estafilococo dorado (sensibles a la meticilina): oxacilina/nafcilina + gentamicina (primera semana) ± rifampicina (si es protésico);
- Estafilococo dorado (SARM): vancomicina ± rifampicina;
- Streptococcus spp.: penicilina G o ceftriaxona ± gentamicina;
- Enterococcus spp.: ampicilina + gentamicina o + ceftriaxona (si HLR a la gentamicina).
Tratamiento quirúrgico
Indicaciones:
- Insuficiencia cardiaca por disfunción valvular (regurgitación valvular aguda grave);
- Infección no controlada (absceso; perforación; pseudoaneurisma; bacteriemia continua >7 días a pesar de una terapia antibiótica adecuada);
- Embolias repetidas o vegetaciones grandes c episodio de embolias (>10 mm), vegetaciones >15 mm, especialmente en EI izquierda incluso sin embolias;
- Endocarditis protésica;
- EI fúngica o causada por microorganismos muy resistentes.
Contraindicaciones:
- Estado general descompensado, fallo multiorgánico;
- Accidente cerebrovascular masivo reciente con componente hemorrágico.
Tipos de operaciones (en la gran mayoría de los casos, las operaciones se realizan con circulación artificial):
- Sustitución (prótesis) de la válvula afectada;
- Eliminación de vegetaciones, saneamiento de abscesos;
- Intervenciones reconstructivas (válvula, anillo valvular, plastia de la raíz aórtica): si la raíz aórtica está afectada, puede ser necesario sustituirla por un conducto (prótesis vascular artificial con válvula artificial) o un homoinjerto (válvula de donante humano con una sección de aorta ascendente);
- Extracción de dispositivos infectados (Si hay electrodos o marcapasos implicados: extracción obligatoria de todo el sistema. En la endocarditis por TAVI: la cirugía suele ser muy letal, pero está indicada si la terapia no es eficaz).
PREGUNTAS FRECUENTES
1. ¿Qué es la endocarditis infecciosa?
2. ¿Qué síntomas son los más característicos de la EI?
3. ¿Qué bacterias causan más frecuentemente la EI?
4. ¿Cuáles son los peligros de la endocarditis infecciosa?
5. ¿Puede tratarse la EI sin cirugía?
6. ¿Cuándo es necesaria la cirugía para la EI?
• Insuficiencia cardiaca por disfunción valvular;
• Abscesos, roturas, perforaciones;
• Terapia antibiótica ineficaz;
• Infección fúngica;
• Émbolos recurrentes.
7. ¿Durante cuánto tiempo se administra el tratamiento antibiótico?
8. ¿Puede prevenirse la endocarditis infecciosa?
9. ¿Quién tiene un riesgo elevado de EI?
Lista de fuentes
1.
Catálogo VOKA.
https://catalog.voka.io/2.
2023 ESC Guidelines for the management of endocarditis. Delgado V, Ajmone Marsan N, de Waha S, Bonaros N, Brida M, Burri H, Caselli S, Doenst T, Ederhy S, Erba PA, Foldager D, Fosbøl EL, Kovac J, Mestres CA, Miller OI, Miro JM, Pazdernik M, Pizzi MN, Quintana E, Rasmussen TB, Ristić AD, Rodés-Cabau J, Sionis A, Zühlke LJ, Borger MA; ESC Scientific Document Group. Eur Heart J. 2023 Oct 14;44(39):3948-4042. doi: 10.1093/eurheartj/ehad193.
3.
Infective endocarditis. Li M, Kim JB, Sastry BKS, Chen M. Lancet. 2024 Jul 27;404(10450):377-392. doi: 10.1016/S0140-6736(24)01098-5.
4.
Infective endocarditis: A contemporary update. Rajani R, Klein JL. Clin Med (Lond). 2020 Jan;20(1):31-35. doi: 10.7861/clinmed.cme.20.1.1.
5.
Management Considerations in Infective Endocarditis: A Review. Wang A, Gaca JG, Chu VH. JAMA. 2018 Jul 3;320(1):72-83. doi: 10.1001/jama.2018.7596.
6.
Infective Endocarditis in Adults: Diagnosis, Antimicrobial Therapy, and Management of Complications: A Scientific Statement for Healthcare Professionals From the American Heart Association. Baddour LM, Wilson WR, Bayer AS, Fowler VG Jr, Tleyjeh IM, Rybak MJ, Barsic B, Lockhart PB, Gewitz MH, Levison ME, Bolger AF, Steckelberg JM, Baltimore RS, Fink AM, O’Gara P, Taubert KA; American Heart Association Committee on Rheumatic Fever, Endocarditis, and Kawasaki Disease of the Council on Cardiovascular Disease in the Young, Council on Clinical Cardiology, Council on Cardiovascular Surgery and Anesthesia, and Stroke Council. Circulation. 2015 Oct 13;132(15):1435-86. doi: 10.1161/CIR.0000000000000296.
7.
Infective endocarditis. Epidemiology, pathophysiology and histopathology. Iung B. Presse Med. 2019 May;48(5):513-521. doi: 10.1016/j.lpm.2019.04.009.
8.
Native-Valve Infective Endocarditis. Chambers HF, Bayer AS. N Engl J Med. 2020 Aug 6;383(6):567-576. doi: 10.1056/NEJMcp2000400.
9.
Infective Endocarditis-Update for the Perioperative Clinician. Jain A, Subramani S, Gebhardt B, Hauser J, Bailey C, Ramakrishna H. J Cardiothoracic Vasc Anesth. 2023 Apr;37(4):637-649. doi: 10.1053/j.jvca.2022.12.030.