Эмбриологические характеристики 8-й недели развития
На 8-й неделе беременности эмбрион приобретает человеческие черты, достигая длины 30 мм. Узнайте, как выглядит плод, какие органы формируются и что показывает УЗИ.
Специальности
АкушерствоАнгиологияАнестезиологияГастроэнтерологияГематологияГепатологияГинекологияГистологияДерматологияИнфекционные болезниКардиологияНеврологияОнкологияОртопедияОториноларингологияОфтальмологияПедиатрияПульмонологияСтоматологияТравматологияУрологияФизиологияЭмбриологияЭндокринологияЭта статья предназначена только для информационных целей
Содержание этого сайта, включая текст, графику и другие материалы, предоставляется исключительно в информационных целях. Оно не является советом или руководством к действию. По поводу вашего конкретного состояния здоровья или лечения, пожалуйста, проконсультируйтесь с вашим лечащим врачом.
Четырнадцатый день постконцепционного развития человека представляет собой один из наиболее значимых этапов раннего эмбриогенеза. В этот период начинается гаструляция, в ходе которой из двухслойного зародышевого диска формируются три зародышевых листка – эктодерма, мезодерма и энтодерма.
Это переходный этап между имплантацией и активной гаструляцией. На этом этапе начинается взаимодействие между эмбрионом и материнским организмом через лакуны синцитиотрофобласта.
Одновременно устанавливаются основные оси тела, которые закладывают план организации будущего организма:
Параллельно с этими процессами продолжается формирование внезародышевых структур, необходимых для нормального обмена между эмбрионом и материнским организмом.
К этому сроку размер эмбрионального диска составляет около 1,5–2 мм. Несмотря на небольшие размеры, диск сохраняет двухслойное строение, но уже активно вступает в фазу перестройки.
Верхний слой представлен эпибластом – высокими цилиндрическими клетками с выраженным апикально-базальным поляритетом и высокой митотической активностью. Эпибласт является источником всех эмбриональных тканей и одновременно формирует стенку амниотической полости.
Его клетки образуют прочные межклеточные контакты за счет экспрессии E-кадгеринов, однако в зоне каудального конца эти связи постепенно ослабляются, что подготавливает эпибласт к миграции.
Нижний слой эмбрионального диска представлен гипобластом, состоящим из уплощенных клеток, образующих тонкую пластинку. Клетки гипобласта не участвуют напрямую в формировании тканей зародыша, но обеспечивают развитие внезародышевой энтодермы и формирование желточного мешка.
Кроме того, они секретируют сигнальные молекулы – LEFTY1, Cer1 и DKK1, которые ингибируют экспрессию WNT и NODAL в краниальной области, что позволяет избежать избыточной мезодермализации и способствует правильному развитию передних структур.
На каудальном конце диска формируется первичная полоска – утолщение эпибласта, которое является первым морфологическим признаком начинающейся гаструляции и задает кранио-каудальную ось эмбриона.
Клетки полоски теряют апикально-базальную полярность, перестраивают цитоскелет с участием Rho-GTPаз и приобретают свойства миграции.
В краниальной части полоски возникает первичный узел (узел Хензена), который служит центром организации. Его клетки секретируют NODAL, FGF8 и WNT3A, активирующие процессы эпителиально-мезенхимального перехода, в результате чего эпибластные клетки начинают активно перемещаться внутрь диска.
Начиная с 14 дня наблюдается миграция эпибластных клеток, которая имеет строго упорядоченный характер.
Таким образом, именно на этом этапе происходит окончательное выделение трех зародышевых листков – эктодермы, мезодермы и энтодермы, что становится основой дальнейшего органогенеза.
В краниальной области диска формируется прекардиальная пластинка — локальное уплотнение клеток мезодермы, которое служит ранним маркером ротовой мембраны и важным ориентиром краниального конца эмбриона.
Параллельно с этими морфогенетическими процессами устанавливаются пространственные оси зародыша.
Ниже представлена подробная схема строения:






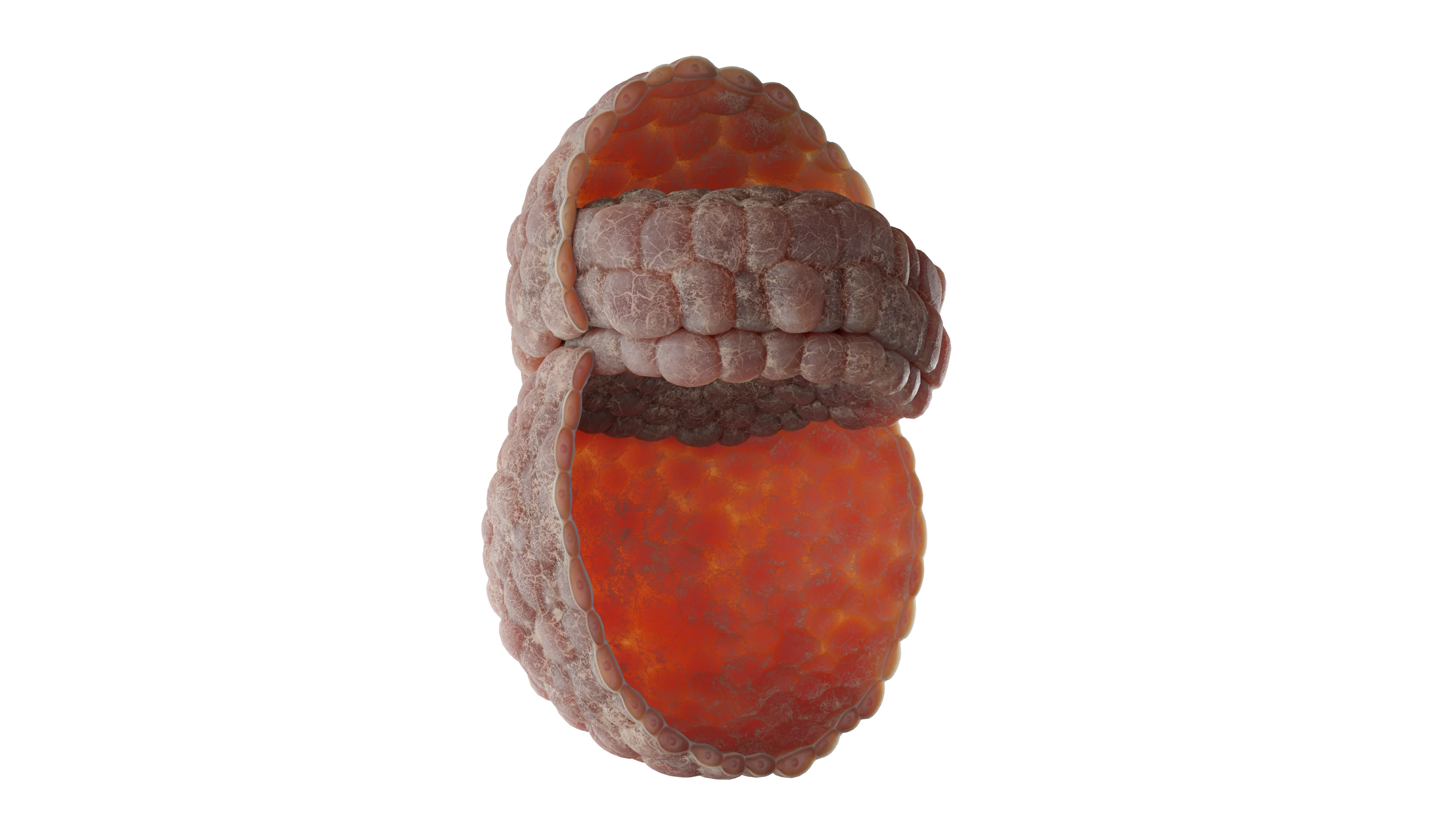





На этом этапе развитие зародыша тесно связано с формированием внезародышевых структур, которые обеспечивают его питание, защиту и закладку будущей плаценты.
Амнион образуется из клеток амниобластов, происходящих из эпибласта. Эти клетки формируют тонкую мембрану, выстилающую амниотическую полость, которая располагается над эпибластом. Амниотическая полость постепенно увеличивается, наполняясь амниотической жидкостью. Уже на данном этапе амнион начинает выполнять защитную функцию, создавая оптимальную среду для развития эмбриона.
К 14-му дню желточный мешок принимает вид вторичного (дефинитивного) мешка. Его стенка выстлана клетками гипобласта и внезародышевой энтодермы. В дальнейшем именно в желточном мешке закладываются очаги первичного кроветворения и формируются зачатки половых клеток.
Несмотря на то, что у человека желточный мешок не участвует в питании эмбриона, он имеет важное значение как источник клеточных линий и временный орган кроветворения.
Хорион формируется из клеток трофобласта и прилежащей внезародышевой мезодермы. На данном этапе в хорионе происходят ключевые изменения, определяющие будущее формирование плаценты. Внедрение трофобласта в эндометрий сопровождается развитием ворсинчатого аппарата: формируются первичные ворсины, которые состоят из центрального слоя цитотрофобласта и покрывающего его слоя синцитиотрофобласта.
В толще синцитиотрофобласта появляются лакуны, которые постепенно заполняются материнской кровью. Этот процесс знаменует собой начало установления примитивного материнско-эмбрионального обмена веществ – первой формы плацентарной циркуляции.
Хотя аллантоис начинает формироваться чуть позже (примерно на 16-й день), уже на этом этапе в каудальной части эмбрионального диска закладывается область, из которой он вырастет. Аллантоис играет важную роль в формировании кровеносных сосудов плаценты и закладке мочевого пузыря.
В эмбриологии развитие человека принято описывать по стадиям Карнеги (Carnegie stages) – это универсальная система классификации, основанная не на возрасте эмбриона в днях, а на его морфологических признаках. Всего выделяют 23 стадии, которые охватывают период от оплодотворения до конца 8-й недели (56-й день).
На данном этапе эмбрион относится к стадия Карнеги 6. В клиническом смысле – это момент, когда эмбрион еще не имеет четких осей тела (голова–хвост, спина–живот), но уже формируются основные внезародышевые структуры, обеспечивающие его дальнейший рост и имплантацию.
Ключевым событием данной стадии является формирование условий для гаструляции, которая начнётся на следующей стадии. Для стадии Карнеги 6 характерно:
Главные процессы включают:
Прогрессия эмбриогенеза по Карнеги (5–7 стадии)
| Стадия 5 (11-13 день) | Стадия 6 (13-15 день) | Стадия 7 (16-19 день) |
|---|---|---|
| Завершение имплантации | Вторичный желточный мешок | Первичная полоска и узел Хензена |
| Двуслойный диск | Амнион | Начало гаструляции |
| Амниотическая полость | Хорион с первичными ворсинами | Хордиальный отросток |
| Первичный желточный мешок | Внезародышевое целомическое пространство | Формирование 3 листков |
| Лакуны в синцитиотрофобласте | Подготовка к гаструляции | Определение осей тела |
Формирование первичной полоски и разделение зародыша на три зародышевых листка осуществляется под контролем сложных сигнальных каскадов.
Ключевым регулятором является система NODAL, необходимая для:
Эффект зависит от уровня экспрессии:
Пространственная активность NODAL строго контролируется его антагонистами – LEFTY1, LEFTY2 и CER1, что предотвращает избыточное образование мезодермы.
Белки WNT3 и WNT3A:
Взаимодействие WNT с BMP4:
Однако требуется строгое равновесие:
Белок FGF8, секретируемый клетками первичной полоски:
В результате клетки эпибласта приобретают способность перемещаться внутрь эмбриона.
Параллельно с этим закладываются оси эмбриона.
В этих процессах участвуют и транскрипционные факторы.
Одновременно продолжается развитие внезародышевых структур. Синцитиотрофобласт секретирует хорионический гонадотропин человека (hCG, кодируется генами семейства CGB), который поддерживает функцию желтого тела и обеспечивает секрецию прогестерона.
Для успешной имплантации и развития плаценты необходимы металлопротеиназы (MMP2 и MMP9), которые разрушают межклеточный матрикс эндометрия и обеспечивают инвазию трофобласта. Факторы VEGF и PGF стимулируют рост сосудистой сети хориона, создавая условия для материнско-эмбрионального обмена.
Наконец, экспрессия HLA-G обеспечивает иммунологическую толерантность матери, блокируя разрушение трофобласта NK-клетками и предотвращая иммунный конфликт.
Таким образом, развитие на этом этапе можно представить как взаимодействие двух систем:
Внезародышевые сигналы (CGB, MMP, VEGF, HLA-G) обеспечивают питание, инвазию и иммунную защиту эмбриона.
1. Можно ли увидеть эмбрион на 2-й неделе по УЗИ?
2. Где находится эмбрион на 2 неделе развития?
3. Каков точный размер эмбриона на 14-й день?
4. Какие симптомы чувствует женщина на 2-й неделе эмбриогенеза?
Список источников
1.
VOKA 3D Anatomy & Pathology — Complete Anatomy and Pathology 3D Atlas [Internet]. VOKA 3D Anatomy & Pathology.
Available from: https://catalog.voka.io/
2.
Sadler TW. Langman’s Medical Embryology. 14th ed. Philadelphia: Wolters Kluwer; 2019.
3.
Moore KL, Persaud TVN, Torchia MG. The Developing Human: Clinically Oriented Embryology. 11th ed. Philadelphia: Elsevier; 2020.
4.
Schoenwolf GC, Bleyl SB, Brauer PR, Francis-West PH. Larsen’s Human Embryology. 6th ed. Philadelphia: Elsevier; 2021.
5.
Deglincerti A, Croft GF, Pietila LN, et al. Self-organization of the in vitro attached human embryo. Nature. 2016;533(7602):251-254.
6.
Shahbazi MN, Jedrusik A, Vuoristo S, et al. Self-organization of the human embryo in the absence of maternal tissues. Nat Cell Biol. 2016;18(6):700-708.
7.
Xiang L, Yin Y, Zheng Y, et al. A developmental landscape of 3D-cultured human pre-gastrulation embryos. Nature. 2020;577(7791):537-542.
8.
Tyser RCV, Mahammadov E, Nakanoh S, et al. Single-cell transcriptomic characterization of a gastrulating human embryo. Nature. 2021;600(7888):285-289.
9.
Petropoulos S, Edsgärd D, Reinius B, et al. Single-cell RNA-seq reveals lineage and X chromosome dynamics in human preimplantation embryos. Cell. 2016;165(4):1012-1026.
10.
Blakeley P, Fogarty NM, del Valle I, et al. Defining the three cell lineages of the human blastocyst by single-cell RNA-seq. Development. 2015;142(18):3151-3165.
11.
Fogarty NME, McCarthy A, Snijders KE, et al. Genome editing reveals a role for OCT4 in human embryogenesis. Nature. 2017;550(7674):67-73.
12.
Rossant J. Genetic control of early cell lineages in the mammalian embryo. Annu Rev Genet. 2018;52:185-201.
13.
Arnold SJ, Robertson EJ. Making a commitment: cell lineage allocation and axis patterning in the early mouse embryo. Nat Rev Mol Cell Biol. 2009;10(2):91-103.
14.
Tam PPL, Behringer RR. Mouse gastrulation: the formation of a mammalian body plan. Mech Dev. 1997;68(1-2):3-25.
15.
Simunovic M, Brivanlou AH. Embryoids, organoids and gastruloids: new approaches to understanding embryogenesis. Development. 2017;144(6):976-985.
16.
Vento-Tormo R, Efremova M, Botting RA, et al. Single-cell reconstruction of the early maternal–fetal interface. Nature. 2018;563(7731):347-353.
17.
Turco MY, Moffett A. Development of the human placenta. Development. 2019;146(22):dev163428.
18.
Aplin JD, Ruane PT. Embryo–epithelium interactions during implantation. J Cell Sci. 2017;130(1):15-22.
19.
Norwitz ER, Schust DJ, Fisher SJ. Implantation and the survival of early pregnancy. N Engl J Med. 2001;345(19):1400-1408.
20.
Wang H, Dey SK. Roadmap to embryo implantation: clues from mouse models. Nat Rev Genet. 2006;7(3):185-199.
21.
Rossant J, Tam PPL. New insights into early human development: lessons from stem cell models. Nat Rev Genet. 2021;22(11):701-713.
Резюме статьи с помощью ИИ
Выберите желаемого помощника ИИ:
Ссылка успешно скопирована
Спасибо!
Ваше сообщение отправлено!
Наши специалисты свяжутся с вами в ближайшее время. Если у вас возникли дополнительные вопросы, пожалуйста, свяжитесь с нами по адресу info@voka.io.