سلائل المعدة: المسببات والتصنيف وطرق والتشخيص والعلاج
هذه المقالة لأغراض إعلامية فقط
يتم توفير محتوى هذا الموقع الإلكتروني، بما في ذلك النصوص والرسومات والمواد الأخرى، لأغراض إعلامية فقط. وليس المقصود منه تقديم المشورة أو التوجيه. فيما يتعلق بحالتك الطبية أو علاجك الخاص، يرجى استشارة مقدم الرعاية الصحية الخاص بك.
السلائل بشكل عام عبارة عن تشكيلات تنشأ من الغشاء المخاطي وتبرز فوقه في أنبوب العضو (وفي هذه الحالة، العضو هو المعدة). تتطلب هذه الحالة المرضية منهجية تمايزية لأن أنواع السلائل المختلفة تتصف باحتماليات متنوعة للتحول الخبيث.
علم الأوبئة
معظم سلائل المعدة هي مكتشفات عرضية في 2% تقريبًا من الدراسات التنظيرية للمعدة التي تُجرى لأسباب أخرى (الفحوصات، وتشخيص أمراض الأعضاء المعنية).
بحسب الدراسات التشريحية المرضية، تُكتشف سلائل المعدة في 0.3–1.1% من الحالات. تشكل السلائل المفرطة التنسج في المعدة ما بين 70–90%. ينشأ المرض بشكل شائع بين سن 40 و 50، ولكنه قد يحدث حتى لدى الأطفال. يتأثر الرجال بالمرض من 2 إلى 4 مرات أكثر من النساء.
تصنيف سلائل المعدة
في المعتاد، يتم تصنيف هذا المرض بناءً على معايير مختلفة، وذلك بناءً على عدد السلائل وشكلها وهيكلها وموضعها، واحتمالية تحولها الخبيث.
حسب العدد
- واحدة؛
- متعددة؛
- تعدد السليلات (يتم التشخيص عند اكتشاف 20 ورمًا أو أكثر لدى الفرد الواحد).
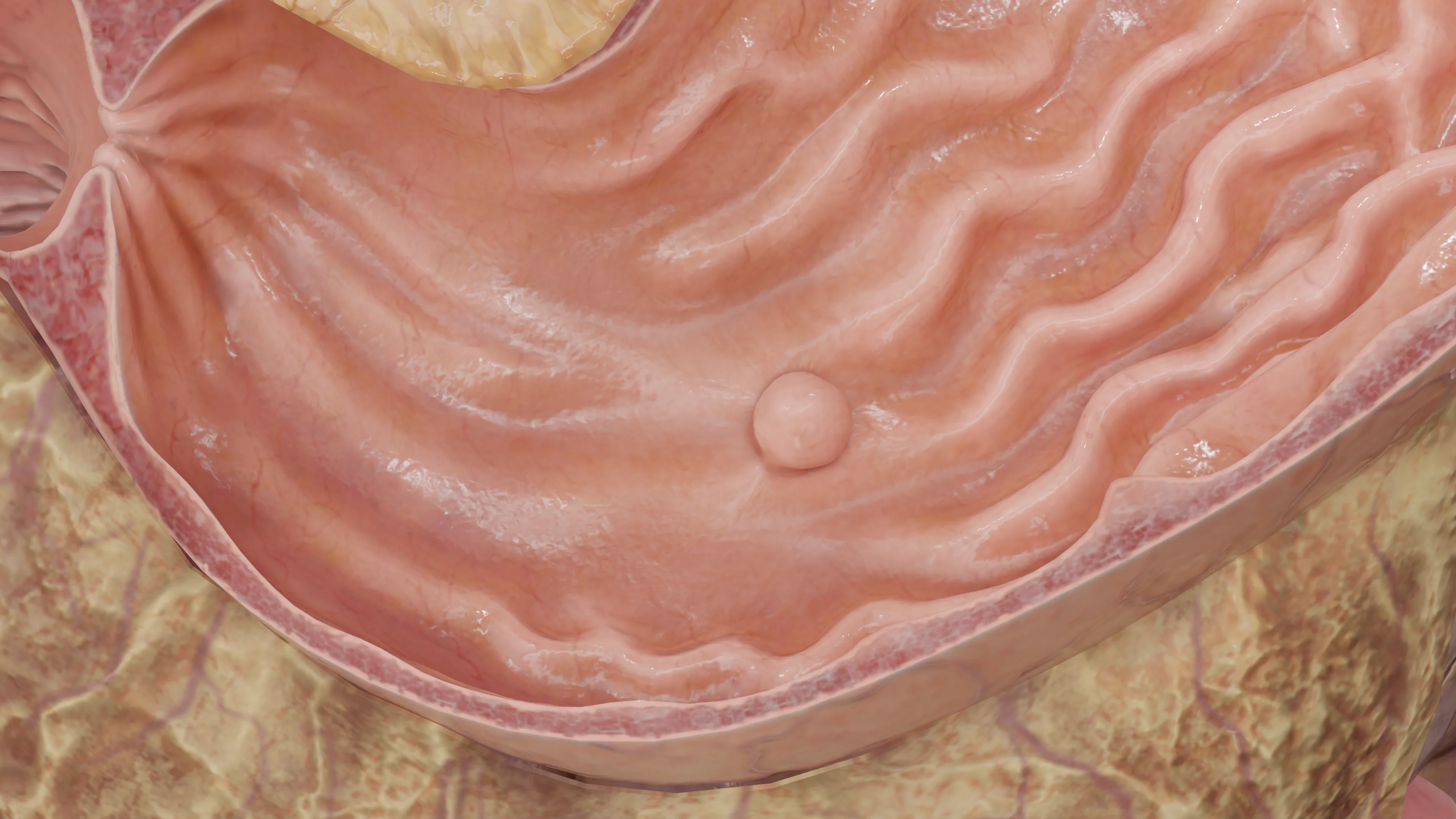

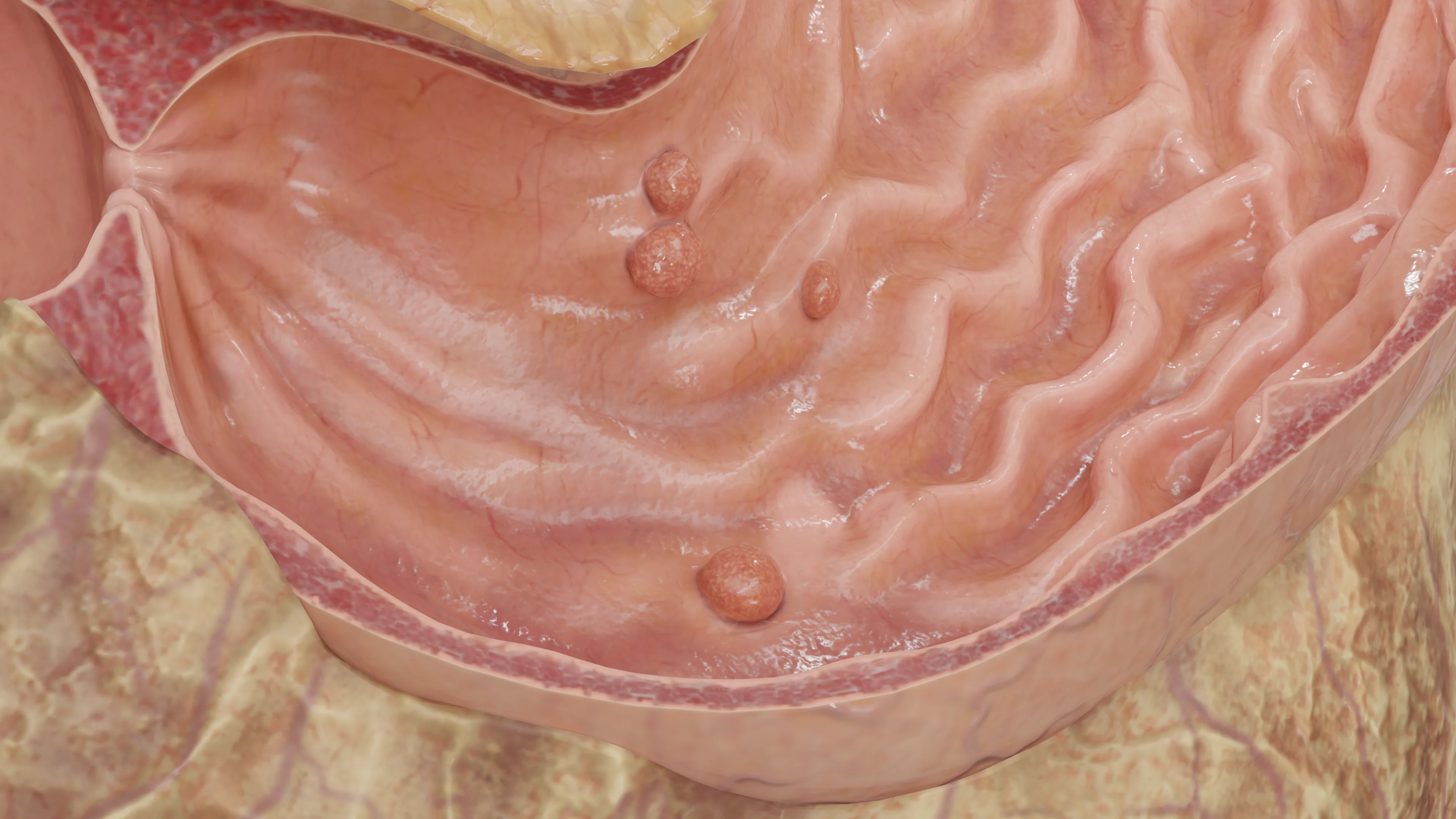

حسب الشكل المجهري
- النوع الأول: هياكل مسطحة مرتفعة فوق الغشاء المخاطي لا تتجاوز 2.5 مم مع حدود غير واضحة؛
- النوع الثاني: يتجاوز الغشاء المخاطي أكثر من 2.5 مم، وله شكل قبة وحدود واضحة؛
- النوع الثالث: مرتفع عن السطح مع قاعدة مندمجة؛
- النوع الرابع: قاعدة ضيقة (سلائل ذات ساق).
حسب احتمالية التحول الخبيث
- سلائل غير ورمية (لا تشمل احتمالية التحول الخبيث): السلائل المفرطة التنسج، والالتهابية، والشبابية (عند الأطفال)، ومتلازمة كرونكايت-كندا؛
- السلائل الورمية (الغدية، السرطاوية، سلائل غدد قاع المعدة).
حسب الموضع
- موضع القلب والوصل القلبي المريئي؛
- جسم المعدة؛
- منطقة الغار؛
- القناة البوطية.
حسب البنية النسيجية
- فرط التنسج؛
- الغدية؛
- الالتهاب الليفي؛
- الأورام العابية؛
- المنتبذات والأورام غير نمطية ذات النمو الورمي (منتبذات البنكرياس، والورم الأصفر، والأورام السدوية المعدية المعوية، والأورام اللمفاوية، وغيرها).
المسببات
الآلية الدقيقة لتشكل السليلات غير معروفة. من الأرجح أن تؤدي آليات عديدة دورًا مهمًا في تشكيلها. اشتملت المواد على شرح ثلاثة نظريات رئيسية لنشأة السلائل:
- النظرية الالتهابية: وجود التهاب مزمن في الغشاء المخاطي (التهاب المعدة المزمن، تفاقم القرحة الدورية). في سياق العملية الالتهابية، يحدث تكاثر مفرط للخلايا لشفاء عيوب الغشاء المخاطي، وهذا قد يشكل السلائل.
- نظرية اختلال التجدد: تشير هذه النظرية إلى استجابة خلايا غير طبيعية (مشوهة، ذات تركيب خلايا مرضي) لتلف الغشاء المخاطي، وهذا يؤدي إلى تكوين تراكم خلايا موضعية مفرطة (أي سلائل).
- النظرية الجنينية: وفقًا لهذه النظرية، تتم التحضيرات جينيًا لظهور السلائل في مرحلة التطور الجنيني. أما خلال تطور الجسم وطوال الحياة، فتظهر السلائل تحت تأثير العوامل الضارة.
وفقًا لعدد من المصادر، قد تؤثر عوامل عديدة ذات نشوء مرضي مختلط أو غير محدد في ظهور السلائل:
- عدوى الملوية البوابية؛
- الاستخدام الطويل الأمد لمثبطات مضخة البروتون؛
- داء السلائل الورمي الغدي العائلي؛
- العادات الغذائية؛
- العمر (لقد تم التأكيد وبائيًا أن حدوث سلائل المعدة تميل للزيادة مع التقدم في العمر).
الصورة السريرية
في المعتاد، تتقدم سلائل المعدة دون أعراض ويتم اكتشافها عرضيًا في أثناء الفحوصات المعتادة للمعدة. تظهر أعراض السليلة القائمة عندما يزداد حجمها غالبًا.
تأتي الأعراض التالية ضمن المظاهر الأكثر تمييزًا للسليلة:
- انزعاج غير محدد في البطن العلوي (غير مرتبط بتناول الطعام)؛
- الشعور بالثقل أو الامتلاء في المعدة؛
- فقر الدم (حتى الوصول إلى فقر الدم الشديد الذي يدفع المريض لزيارة الطبيب) نتيجة لتقرح السليلة وقد ينشأ فقدان الدم المزمن الطويل؛
- القيء الدموي أو الميلينا (عند تدمر السليلة وتسبب تلف الأوعية المغذية، وهذا يؤدي إلى نزيف حاد ضخم مستمر)؛
- انسداد الأمعاء العالي (ألم انتيابي في المنطقة الشرسوفية ينتشر عبر البطن، وقيء الطعام الذي تم تناوله، وغير ذلك) عند اختراق سلائل كبيرة الحجم ونحيفة لقاعدة الاثني عشر وعرقلتها لقناة البواب؛
- التهاب البنكرياس الثانوي (تقارير نادرة في المواد الطبية عن تدلي الأورام الحميدة المفرطة التنسج الكبيرة إلى الاثني عشر، وهذا يسبب انسداد حليمة فاتر [الحليمة الاثني عشرية الكبرى])؛
- فقدان الشهية أو فقدان الشهية؛
- الغثيان؛
- القيء؛
- التهاب المريء بالارتجاع أو حرقة المعدة؛
- عسر البلع أو صعوبة في البلع.
التشخيص
وفقَ الموصوف أعلاه، يتم اكتشاف الأورام الحميدة في المعدة عادةً خلال إجراء تنظير المريء والمعدة والاثنى عشر (esophagogastroduodenoscopy, EGD)، رغم وجود إمكانية للتشخيص عبر التصوير الإشعاعي للمعدة (يظهر خلل في حدود الغشاء المخاطي للمعدة).
تتيح الموجات فوق الصوتية قيمة تشخيصية، وذلك مع أن دقة هذا الفحص ليست عالية. كما يمكن تحديد هذا المرض عند إجراء التصوير المقطعي المحوسب (CT) أو التصوير بالرنين المغناطيسي (MRI) للبطن (مع التحضير الجيد والتصوير المتباين للجهاز الهضمي).
علاج بوليبات المعدة
يتم تحديد اختيار طريقة العلاج بناءً على حجم الورم وخصائصه النسيجية وحدوث مضاعفات سريرية.
إستراتيجية المراقبة والعلاج التحفظي
تجب مراقبة الأورام الحميدة الصغيرة (حتى 5 مم) بشكل دوري كل ستة أشهر. يتم اتباع الإستراتيجية نفسها في حال رفض المريض التام لاستئصال الأورام الحميدة.
يوصي بعض المؤلفين ببدء العلاج التحفظي (استئصال العدوى الملوية البوابية، مثبطات مضخة البروتون) مع إجراء فحص متابعة، وذلك لأن بعض الأورام الحميدة تتناقص وتختفي على مر الزمن (الأورام الحميدة المفرطة التنسج، الأورام الحميدة الالتهابية الليفية).
الجراحة التنظيرية
تعتبر الأورام الحميدة التي يزيد حجمها عن 5 مم والحالات المعقدة (مثل التآكل، أو انسداد الجهاز الهضمي، أو النمو السريع للورم في أثناء المتابعة) مؤشرات للجراحة.
عند اختيار طريقة الجراحة، من الضروري تحديد الهيكل النسيجي للورم. حاليًا، الطريقة المثلى والأكثر قابلية للتطبيق هي استئصال الأورام الحميدة بالمنظار. توجد طرائق عديدة لهذا النوع من استئصال الأورام الحميدة:
- الإزالة بالكهرباء باستخدام حلقة؛
- الإزالة في الطبقة تحت المخاطية؛
- التخثر المباشر للأورام الحميدة الصغيرة.
يقرر مُختص التنظير اختيار طريقة الإزالة بناءً على مجموعة عوامل (حجم وموضع الورم، ونتائج الخزعة، وتوفر المعدات، ومؤهلات الطبيب).
يجب على المرضى الذين خضعوا لاستئصال الأورام بالكهرباء إجراء التنظير بعد 3 و 6 و 12 من الأشهر، ثم يُفضل إجراء التنظير مرة واحدة سنويًا.
الجراحة المفتوحة
تخضع الأورام الحميدة الكبيرة التي لا يمكن إزالتها بالمنظار للجراحة المفتوحة. تشمل هذه الحالات:
- الأورام الحميدة على قاعدة واسعة؛
- الأورام الحميدة ذات احتمالية النزيف العالية؛
- في حالات النتائج الخبيثة من الفحص النسيجي.
يمكن إجراء استئصال اسفيني لجدار المعدة مع الورم، أو استئصال جزئي للمعدة بدرجة أكبر أو أقل اعتمادًا على الخلاصة النسيجية ومدى تأثير المعدة.
أنواع معينة من الأورام الحميدة في المعدة وخصائص إدارتها
الأورام الحميدة ذات الحد الأدنى لاحتمالية التحول الخبيث (غير الورمية)
الأورام الحميدة المفرطة التنسج (التضخمية المنشأ)
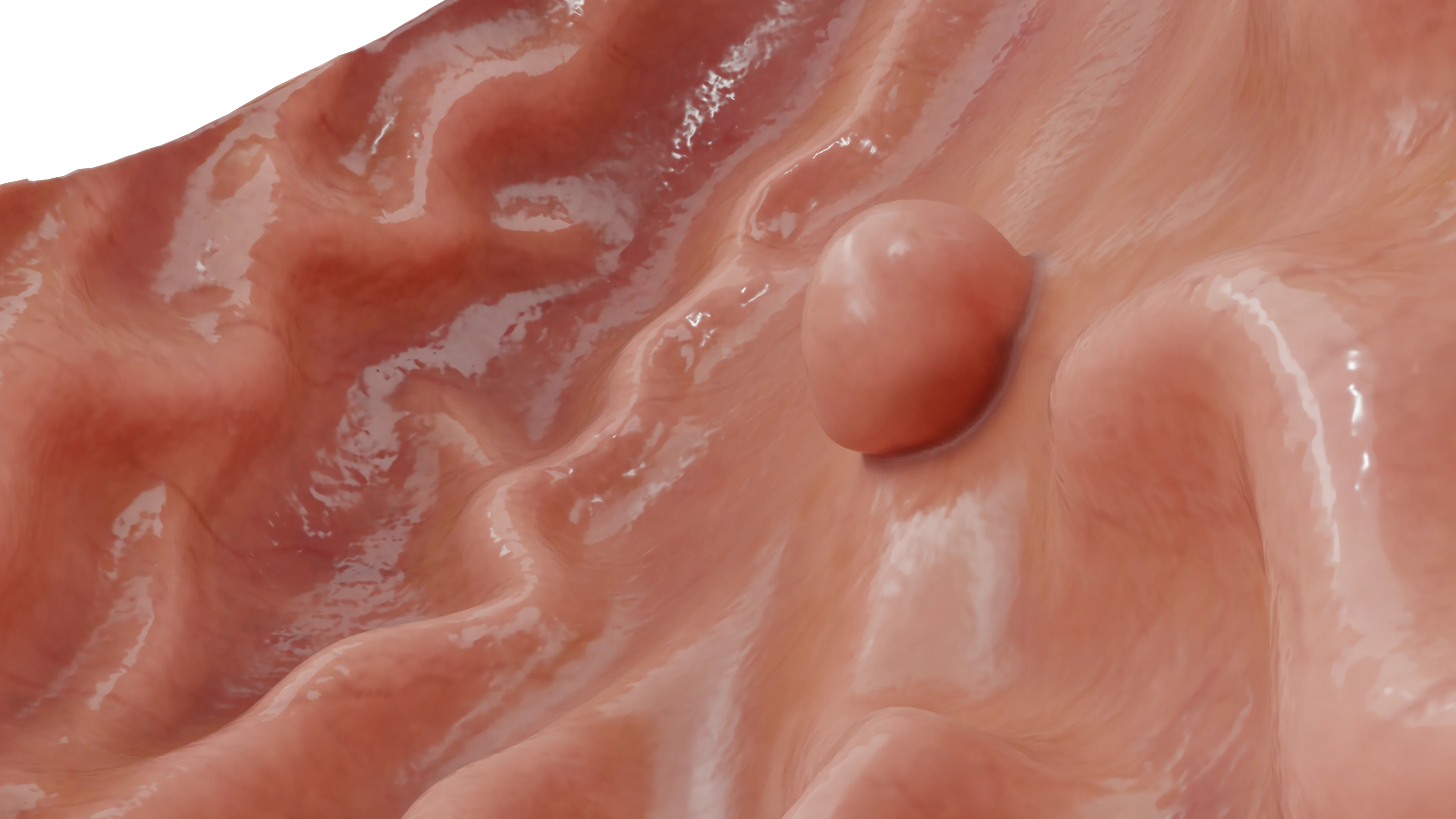

قد تكون إما على قاعدة ضيقة (ذات ساق) أو قاعدة واسعة. يمكن توزيعها بشكل عشوائي في أي جزء من المعدة (من 24% إلى 60% من الأورام الحميدة المفرطة التنسج توجد في منطقة الغار، من 29% إلى 56.3% في جسم المعدة، و2.5% تقريبًا فقط في الكارديا). توجد غالبًا في الفئة العمرية الأكبر سنًا (متوسط العمر 65.5–75 عامًا). توجد ميول طفيفة لدى الإناث، إذ يشكلن 58% إلى 70.5% من المرضى.
تعتبر الأورام الحميدة المفرطة التنسج حالات منفردة في ثلثي الحالات تقريبًا. غالبية الأورام يقل حجمها عن 1 سم، ولا توجد أورام أكبر من 2 سم لدى أكثر من 10% من الحالات. يُعتقد أنها ناتجة عن التجدد الزائد خلال إصابة الغشاء المخاطي المزمنة، وبالتالي تظهر غالبًا في التهاب المعدة المزمن المرتبط بـالملوية البوابية (25% من الحالات)، وفقر الدم الوبيل، وذلك بالقرب من القرحة أو التآكلات أو في مواقع ارتباط المعدة والأمعاء، وأيضًا في موضع تقاطع المريء والمعدة (لدى المرضى الذين يعانون من مرض ارتجاع المريء GERD).
نسيجيًا، تظهر في الأورام الحميدة المفرطة التنسج استطالة الحفريات المعدية مع تشكّل تفرعات، نمو مفرط للصفيحة الخاصة مع تسرب من الخلايا البلازمية، الخلايا الليمفاوية، الحمضات، الخلايا المجهرية، الخلايا البالعة وكميات متفاوتة من العدلات. الغدد المعدية لا تشارك في تشكيل الأورام عادةً. مع الوقت، قد تزداد الأورام الحميدة المفرطة التنسج أو تنكسر (بشكل تلقائي أو بعد القضاء على الملوية البوابية Helicobacter pylori). التحول الخبيث نادر جدًا (1.5%–3% من الحالات، عادةً عندما يصبح الحجم أكبر من 2 سم). لذلك، يجب استئصال الأورام الأكبر حجمًا بالمنظار تمامًا.
الورم الحميد الليفي الالتهابي (الورم الحُبَيبي الحمضي، ورم فانك)
تتصف هذه الأورام بزيادة عدد الخلايا المغزلية الشكل، والخلايا الالتهابية، والأوعية الدموية الصغيرة، ومع سيادة خلايا الحمضات غالبًا. تحدث هذه الأورام في الجهاز الهضمي بالكامل ولكن تُركز بشكل أكبر في المنطقة المعدية البوابية (80%).
تشير المسببات إلى سبب تحسسي، كما يُلاحظ ارتباطها بنقص حموضة المعدة أو انعدامها (مع التهاب المعدة الضموري). يتم تشخيصها بشكل متساوٍ لدى الجنسين في أي سن. توجد الأورام الليفية الالتهابية في الطبقة تحت المخاطية عادةً، على الرغم من أنه وُصفت حالات تؤثر على المخاطية فقط. تتكون من أوعية دموية صغيرة محاطة بخلايا مغزلية الشكل قصيرة قد تُرتب حول الأوعية الأكبر مثل “قشرة البصل”.
أحيانًا تُلاحظ خلايا عملاقة عديدة النوى، تُشبه “الزهور”، ذات أنوية فائقة الكرومية. جميع البنى الموصوفة محاطة بارتشاح خلوي التهابي مزمن مع غلبة الحمضات. يتم اكتشاف مثل هذه الأورام بالصدفة ولا تتصف بأعراض مميزة، وعادةً لا تتكرر بعد الإزالة (ولذلك تُعد الإزالة بالمنظار علاجًا كافٍ).
الورم الأصفر/ اللويحة الصفراء
تُكتشف هذه الآفات غير ذات الأهمية السريرية بصورة أعلى انتشارًا لدى الرجال مع التقدم في السن مقارنةً بالنساء، وترتبط بالتهاب المعدة المزمن واعتلال المعدة وارتداد الصفراء الاثني عشري المعدي. بشكل مجهري، تظهر على شكل آفات فردية أو متعددة قُطرها يتراوح بين 1 إلى 2 مم، مستديرة أو بيضاوية، ومحددة بوضوح صفراء، أو مبقعة، أو عقيدات.
تحدث بشكل أعلى انتشارًا على امتداد القَوس الأصغر. نسيجيًا، تتكون من مجموعات من البالعات الناضجة المحملة بالدهون، والتي تحتل الصفيحة الخاصة وتحتوي على الكوليسترول والدهون المحايدة.
ورم حميد من خلل التنسج العابي من نوع بيوتز-يجرز
قد يشارك الغشاء المخاطي المعدي في داء السلائل بويتز-يجرز (مع أن إصابة الأمعاء الدقيقة والغليظة أعلى انتشارًا). يتكون هذا النوع من السلائل من غدد مفرطة التنسج مبطنة بظهارة من نوع الحفريات المعدية وتفصلها خلايا عضلية ناعمة مع ضمور في المكونات الغدية العميقة.
السلائل اليانعة
تٌعد سلائل المعدة اليانعة الشبابية نادرة وتنشأ غالبًا في سياق مرض السليلات اليانعة سواءً في المعدة فقط أو في كامل الجهاز الهضمي (مع أو بدون حالات عائلية). قد تحدث في أي سن وتتصف عادة بفقر الدم أو نقص بروتينات الدم، وتوجد في الغار عادةً. تتكون من مخاطية متورمة مع تغيرات التهابية، واستطالة ملحوظة، وتعرُّج، وتوسع كيسي في المواضع الحفرية (لذا قد يتم التعرف عليها بشكل خاطئ على أنها سلائل مفرطة التنسج).
السلائل الورمية (تشمل احتمالية التحول الخبيث)
سلائل الغدد القاعدية
تُعد سلائل الغدد القاعدية (FGPs) أورامًا صغيرة مسطحة تحدث بشكل حصري في القاع والجزء العلوي في جسم المعدة. تحدث سلائل الغدد القاعدية بشكل متقطع، مع أنها توجد لدى المرضى الذين يعانون من سلائل الورم الغدي العائلية.
تظهر هذه السلائل في الفحص التنظيري الشفاف كسلائل مسطحة بقطر أقل من 1 سم، متعددة عادةً. قد تظهر لدى الرجال والنساء في أي عمر بنسب متساوية من الحالات. تم توثيق ارتباط سلائل الغدد القاعدية مع العلاج بمثبطات مضخة البروتون (لأكثر من 36 شهرًا)، وهو موضوع خاضع للنقاش بحسب بعض المؤلفين.
في معظم الحالات، تُكشف طفرات جسدية منشّطة (في مواقع الفسفرة لـGSK-3β) لإكسون 3 لجين β-كاتينين في النسيج الحفري والغدي. تتكون سلائل الغدد القاعدية من غدد متوسعة كيسيًا مبطنة بنسيج قاعدي، ممزوجةً بغدد طبيعية، وقد تشمل خلايا عضلية ملساء موزعة بشكل منتشر وفوضوي حول الغدد.
الورم الغدي (السلائل الغدية)
تُعرف منظمة الصحة العالمية (WHO) الأورام الغدية المعدية بأنها آفات محدودة تتكون من هياكل أنبوبية و/ أو زغبية مبطنة بنسيج خلوي مُعتل. يتراوح انتشار الورم الغدي المعدي من 0.5% إلى 3.75% في بلدان نصف الكرة الأرضية الغربي، بينما في البلدان ذات الاحتمالية العالية للسرطان المعدي ويتراوح من 9% إلى 20%.
يزداد تكرار حدوثها مع تقدّم العمر، وتوجد زيادة في حدوثها لدى الأفراد الذين يعانون من متلازمة السلائل الغدية العائلية. تظهر هذه الأورام عادة في سياق التهاب المعدة الضموري مع التحول المعوي، وتوجد في أغلب الأحيان في منطقة الغار، مع كون زاوية المعدة والقاع ثاني أكثر المواضع شيوعًا.
غالبية هذه الأورام تكون منفردة، مرتفعة من الخارج (سواءً أكانت مسطحة أو على قاعدة ضيقة). نادرًا ما تكون “مسطحة” أو حتى منخفضة عن القشرة المحيطة بالغشاء المخاطي. عادةً تكون بحجم 3 إلى 4 سم. تتصف الأورام الغدية في المعدة بسطح مخملي زاوٍ يبرز مقارنة بالغشاء المخاطي الأملس والضموري المحيط.
يمكن تصنيف الأورام الغدية في المعدة حسب درجة التنسج (منخفضة أو عالية) بناءً على كثافة النوى، وفرط التصبغ، والنشاط الانقسامي، والتمايز الخلوي، ودرجة الانحراف النمطي البنيوي. في المعتاد، تتكون الأورام الصغيرة الساقية الأقل من 1 سم من نسيج أنبوبي ضعيف التمايز.
الأورام الغدية الأكبر حجمًا تكون في أغلب الأحيان زغبية مع درجة عالية من خلل التنسج، وتحمل نسبة كبيرة منها تحولًا سرطانيًا. تصل النسبة الخبيثة للأورام الأكبر من 2 سم إلى 40-50%. باعتبارها أورامًا غير متغلغلة مع احتمال التحول إلى سرطان غدي، يجب علاج الأورام الغدية المعدية عن طريق الإزالة الموضعية، وذلك عادةً بعملية استئصال السلائل التنظيرية أو استئصال الغشاء المخاطي التنظيري.
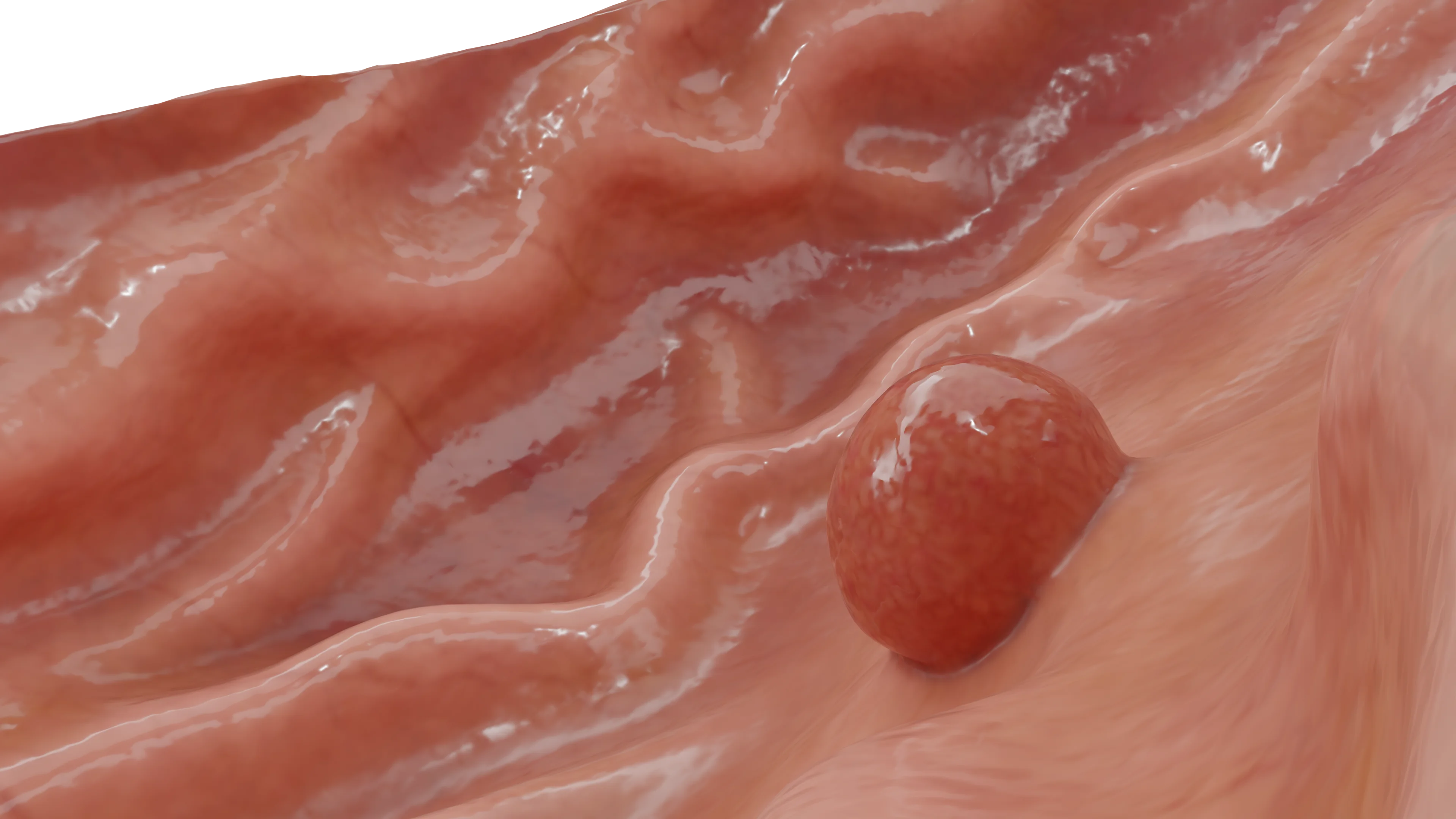

الورم السرطاوي في المعدة
تُعرّف منظمة الصحة العالمية (WHO) الأورام السرطاوية المعدية بأنها أورام غدية صماء جيدة التمايز تتكون من خلايا شبيهة بالمعوية أليفة الكروم غير الوظيفية تنشأ في الغشاء المخاطي المفرز للحمض في جسم أو قاع المعدة.
تُعد الأورام السرطاوية المعدية نادرة حيث تشكّل أقل من 0.5% من جميع الأورام المعدية (أعلى انتشارًا لدى المرضى الذين يعانون من التهاب معدي ضموري مناعي ذاتي مع متلازمة زولينجر-إليسون المصاحبة، وبشكل متقطع أحيانًا). الأورام منفردة وقد تظهر عليها سمات مشابهة لسمات السرطان (مثل نزيف الجهاز الهضمي، أو الانسداد، أو النقائل). تظهر في الأورام السرطاوية المعدية أنماطًا شريطية أو عظمية مُنظمة مع تنظيم جزيري النمط. يمكن للورم السرطاوي الكبير الانتقال إلى العقد اللمفاوية والكبد، وكذلك لأعضاء أخرى أكثر بعدًا. مع ذلك، يكون نموه بطيئًا عادةً.
يرتبط الحجم والقدرة الاجتياحية ارتباطًا وثيقًا باحتمالية حدوث النقائل. تتصف الأورام السرطاوية التي تقل حجمها عن 2 سم والعديد منها باحتمالية انتقال منخفض جدًا، في حين قد تبقى الأورام التي يقل قُطرها عن 1 سم مستقرة لسنوات عديدة ودون نمو غالبًا.
يوصى باستئصال الأورام التي يزيد قُطرها عن 2 سم، نظرًا لأنها تتصف باحتمالية كبيرة للاجتياح اللمفاوي والانتقالات. يُعد علاج الأورام السرطاوية السطحية الصغيرة المتعددة أكثر تحديًا؛ إذ تُمكن إزالة الأورام بدقة عن طريق التنظير، ولكن يوصي بعض المؤلفين باستئصال المعدة أو استئصال منطقة الغار (فهذا يقضي على فرط جاسترين الدم ويؤدي إلى تراجع الآفات المفرطة التنسج وربما الإصابة بالورم السرطاوي).
الأسئلة الشائعة
1. فيم تتمثل السلائل المعدية؟
2. ما أسباب ظهور السلائل في المعدة؟
3. فيم تتمثل الأعراض التي قد تشير إلى وجود السلائل؟
4. هل تتحول السلائل المعدية إلى سرطان دائمًا؟
5. هل يمكن علاج السلائل بدون جراحة، وهل يمكن أن تختفي من تلقاء نفسها؟
6. في أي الحالات تكون إزالة السلائل ضرورية؟
7. ما كيفية إزالة السلائل؟
8. فيم تتمثل الحمية الغذائية اللازمة للسلائل المعدية؟
قائمة المصادر
1.
VOKA 3D التشريح & علم الامراض – Complete Anatomy and Pathology 3D Atlas [Internet]. VOKA 3D التشريح&علم الامراض.
Available from: https://catalog.voka.io/ متاح
2.
Abraham SC, Park SJ, Lee JH, Mugartegui L, Wu TT. “Genetic alterations in gastric adenomas of intestinal and foveolar phenotypes” (التغيرات الجينية في الأورام الغدية المعدية ذات الأنماط الظاهرية المعوية والنقيرية) Mod Pathol. 2003;16: 786–795.
3.
Bosman FT, Carneiro F, Hruban R, Theise N (2010) “WHO Classification of Tumours of the Digestive System” (تصنيف منظمة الصحة العالمية لأورام الجهاز الهضمي), (4th edn), International Agency for Research on Cancer (IARC), Lyon, 2010.
4.
Delle Fave G, Kwekkeboom DJ, Van Cutsem E, Rindi G, Kos-Kudla B, et al. (2012) “ENETS Consensus Guidelines for the Management of Patients with Gastroduodenal Neoplasms” (دليل إجماع ENETS لإدارة المرضى الذين يعانون من الأورام الازدواجية للمعدة والاثني عشر) Neuroendocrinology 95: 74–87.
5.
Lim SA, Yun JW, Yoon D, Choi W, Kim SH, et al. (2011) “Regression of hyperplastic gastric polyp after Helicobacter pylori eradication” (تراجع الورم الحميد المفرط التنسج في المعدة بعد استئصال بكتيريا الملوية البوابية) Korean J Gastrointest Endosc 42: 74-82.
6.
Pantanowitz L, Antonioli DA, Pinkus GS, Shahsafaei A, Odze RD. “Inflammatory fibroid polyps of the gastrointestinal tract: evidence for a dendritic cell origin” (السلائل الليفية الالتهابية للجهاز الهضمي: دليل على الأصل الخلوي الشجري) Am J Surg Pathol. 2004;28:107–114.
7.
Park DY, Lauwers GY (2008) “Gastric polyps: classification and management” (سلائل المعدة: التصنيف والإدارة) Arch Pathol Lab Med 132: 633-640.
8.
Ramage JK, Ahmed A, Ardill J, Bax N, Breen DJ, et al. (2012) “Guidelines for the Management of Gastroenteropancreatic Neuroendocrine (Including Carcinoid) Tumours (NETs)” (إرشادات لإدارة الأورام العصبية الصماء للجهاز الهضمي والبنكرياسي (NETs) بما في ذلك السرطانات الصغيرة) Gut 61: 6–32.
9.
Torbenson M, Lee JH, Cruz-Correa M, et al. “Sporadic fundic gland polyposis: a clinical, histological, and molecular analysis” (داء السلائل الغدية للفؤاد المتناثر: تحليل سريري، وتشريح نسيجي، وتحليل جزيئي) Mod Pathol. 2002;15:718– 723.
10.
Belonogov A.V., Zhitov D.I. “Endoscopic and endosurgical methods of treating stomach polyps” (in Russian) (الطرق التنظيرية والجراحية التنظيرية لعلاج سلائل المعدة), Bulletin of Siberian Branch, Russian Academy of Medical Sciences, vol. 2, No. 5, pp. 76–79, 2002.
11.
Blok B., Schakhmal G., Shmidt G. “Gastroscopy” (تنظير المعدة) (In Russian) Moscow: MED press-inform, 2007, 216 p. (Trans. from Ger. under general editorship of I. V. Maev, S. I. Emelyanov).
12.
Tereshchenko S.G. “Optimization of intra-organ interventions for the prevention of bleeding in operative endoscopy for digestive tract diseases (in Russian)” (التنظيم الأمثل للتدخلات داخل الأعضاء للوقاية من النزيف في التنظير الجراحي الطارئ لأمراض الجهاز الهضمي) Moscow: Moscow Regional Research and Clinical Institute, 2015. — 23 с.
13.
Khomyakov V.M., Ermoshina A.D., Pirogov S.S., Ryabov A.B. “Modern views on risk factors for gastric cancer” (الرؤى الحديثة لعوامل الخطر لسرطان المعدة) (in Russian), Russian Journal of Gastroenterology, Hepatology and Coloproctology, vol. 27, no. 6, pp. 78–86, 2017.